¿Por qué conducen la electricidad los metales? La física cuántica tiene la clave
Los metales son muy buenos conductores de la electricidad y del calor y el motivo se esconde en los mismos principios de la física cuántica. Estos materiales han sido imprescindibles durante la historia de la humanidad, pero hasta hace pocas décadas no sabíamos por qué.

Los metales han definido la historia de la humanidad. Tanto, que varios periodos en la frontera entre la historia y la prehistoria humanas reciben su nombre porque fue durante esas épocas que comenzamos a poder trabajarlos. La edad de bronce y más tarde la de hierro asentaron nuestro dominio sobre la naturaleza, nuestra capacidad de alterar el entorno que nos rodea y de sobreponernos a las limitaciones de nuestra propia biología para construir un mundo más complejo.

Museo Nacional de Corea | Artefactos de bronce encontrados en Corea
Esta relación no ha dejado de ser fructífera, por supuesto. La sociedad actual no podría existir sin nuestro profundo conocimiento de incontables materiales, entre los que los metales han jugado un papel decisivo. Desde herramientas a la propia infraestructura sobre la cual producimos o transportamos la energía que mueve el mundo, los metales son hoy más importantes que nunca. Una de sus características más importantes, especialmente en los últimos siglos, es su capacidad para conducir la electricidad.

Una chispa salta entre dos cables de cobre. Foto: Istock
Esta conductividad eléctrica es consecuencia de su estructura atómica. En los metales, los átomos se disponen en una red cristalina compacta y ordenada, con gran cantidad de electrones formando una especie de envoltura alrededor del metal. Este mar de electrones es precisamente el responsable de que puedan conducir la electricidad de manera tan eficiente. Los electrones que se encuentran libres en este mar, se mueven con facilidad a través de la superficie del metal. Si aplicamos una diferencia de potencial, un voltaje, al metal, conectando cada extremo a uno de los polos de una pila, los electrones fluirán hacia el polo positivo, creando con su movimiento una corriente eléctrica.
Por supuesto cada metal será diferente y mostrará una conductividad diferente. La plata, el cobre, el aluminio y el oro son materiales especialmente conductores y cada uno tiene su uso en nuestra sociedad. La plata, por ejemplo, es mejor conductor que el cobre, pero también resulta mucho más cara de conseguir y por eso se utiliza el cobre para construir el cableado que transmite la corriente eléctrica de las centrales a nuestras casas o industrias.
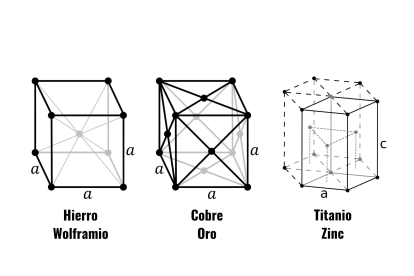
Wikimedia Commons | Estructura cristalina presente en algunos metales
El mar de electrones y su capacidad para conducir la electricidad es una consecuencia directa de las leyes de la física cuántica. Como también ocurre en un átomo, los electrones en un metal no pueden ocupar cualquier estado energético, sino que tendrán unas energías definidas que podrán ocupar. La diferencia entre los átomos aislados y la red formada por un metal es que en este segundo caso pueden existir una gran cantidad de niveles energéticos muy próximos entre sí. Cuando varios niveles aparecen juntos forman lo que se conoce como una banda. La última banda que contenga electrones probablemente no estará llena. Los niveles más bajos estarán constantemente llenos, pero los más altos estarán llenos o vacíos, en función de la cantidad y la energía de los electrones presentes.
En un material conductor, los electrones presentes llenarán la última de estas bandas hasta aproximadamente la mitad, de forma que haya aún muchos huecos que podrán ocupar. En un material aislante, la última banda estará completamente llena y la siguiente quedará muy lejos como para que los electrones puedan saltar a ella, de forma que no tendrán libertad de movimiento y no podrán conducir la electricidad.
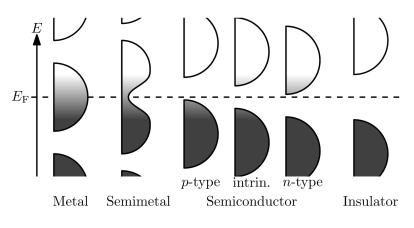
Nanite | Representación simplificada del modelo de bandas que explica las propiedades conductoras o aislantes de diferentes materiales
La propiedad que da a los metales la capacidad de conducir la electricidad es la misma que les hace tan buenos conductores térmicos. La misma libertad de movimiento que permite a los electrones crear una corriente eléctrica, también les permite almacenar energía térmica, consiguiendo que los metales no sean solamente buenos conductores de la electricidad si no también del calor. Al fin y al cabo, la temperatura es una manifestación de la energía cinética media de las partículas que componen un determinado material.
Es decir, cuanto más caliente esté un objeto, más rápido se moverán las partículas que lo componen. Esto significará que tanto los átomos que forman la red tridimensional como los electrones que la rodean aumentarán su velocidad con la temperatura. Los electrones, al tener mayor libertad de movimiento, podrán transferir esta energía cinética a otro material con el que entren en contacto, como por ejemplo tu piel si tocas un metal caliente.

Alchemist-hp | El hierro fue uno de los metales más importantes en la antigüedad
Fue de hecho su conductividad térmica lo que hizo a los metales imprescindibles para el ser humano por primera vez, además de otras propiedades plásticas. Al ser tan buenos conductores térmicos, podían calentarse fácilmente, lo cual permitía fundirlos y otorgarles diferentes formas para crear herramientas, utensilios o armas. Esto hizo que multitud de civilizaciones antiguas ganaran un gran conocimiento de diferentes metales y los incorporaran a su actividad diaria, lo que nos permitió, llegado el momento, ir más allá y conocer sus propiedades eléctricas.
A lo largo de los siglos XVIII y XIX multitud de investigadores investigaron las propiedades eléctricas y magnéticas de diversos metales, lo que desembocaría en las ecuaciones de Maxwell para el electromagnetismo, la construcción de una bombilla barata, eficiente y duradera por Thomas Alba Edison y multitud de inventos y descubrimientos relacionados, que nos han permitido llegar hasta el nivel de desarrollo tecnológico actual.
Referencias:
- Ashcroft, Neil and N. David Mermin, Solid State Physics, ISBN 0-03-083993-9
- Griffiths, D. J. (2008). Introduction to electrodynamics. Pearson.